Soluções de energia em medicina - Normas oferecem segurança
2018-07-26
Pessoas e energia elétrica não se misturam bem, e isso é especialmente verdade quando as pessoas são pacientes – seja em uma instalação médica ou, cada vez mais, em um ambiente doméstico. A fim de garantir a segurança tanto dos pacientes quanto dos profissionais de saúde, o mercado dos serviços de saúde é fortemente regulamentado por uma série de requisitos baseados em normas e testes de produtos associados.
O fundamental para o regime de normas é a IEC 60601, que é composta de um conjunto de requisitos específicos para os equipamentos elétricos e eletrônicos utilizados na área da saúde. Publicada originalmente há cerca de 40 anos, a IEC 60601 tem acompanhado as mudanças do setor.
Neste artigo técnico, examinamos alguns dos princípios fundamentais da IEC 60601, na medida em que se referem à implementação de fontes de alimentação, bem como alguns dos novos requisitos, tais como a necessidade de avaliação de risco. Além disso, formas práticas de alcançar a conformidade serão analisadas, tais como o suporte disponível para os fabricantes de dispositivos médicos.
Introdução
Uma das principais preocupações de segurança com relação aos dispositivos médicos é que o paciente está, muitas vezes, conectado eletricamente ao dispositivo. Um exemplo disso são os eletrodos de um eletrocardiógrafo. Na IEC 60601, estas são definidas como "peças aplicadas" (AP) e são uma definição importante dentro da norma ao definir os requisitos gerais de um produto médico.
Os dispositivos médicos devem incorporar pelo menos um Meio de Proteção (MOP) para assegurar que tanto o paciente, se conectado através de um AP, quanto o operador estejam protegidos contra os riscos de choque elétrico, mesmo em condições de falha. Um MOP pode ser alcançado através de uma isolação de segurança, um terra de proteção, um caminho de fuga definido, uma folga de ar, outras impedâncias de proteção ou pela implementação de uma combinação destas técnicas.
Na norma, os operadores e pacientes são tratados de forma diferente, resultando nas classificações 'Meios de Proteção do Operador' (MOOP) e 'Meios de Proteção do Paciente' (MOPP). Uma razão para esta diferença é que o paciente pode estar fisicamente conectado através de um PA e inconsciente quando a falha ocorre. Devido a este risco, os requisitos do MOPP são os mais rigorosos dos dois. Cada termo é definido em termos de tensão de isolação, distância do caminho de fuga e nível de isolação.
|
||||||||||||||||||||||||
Figura 1: definições de MOOPs e MOPPs para a norma IEC 60601 (Fonte da imagem: TRACO Power)
Normas em evolução
A IEC 60601 evoluiu desde sua primeira publicação há quase 40 anos. Como as fontes de alimentação e os módulos não são dispositivos médicos em si, as normas não se aplicam diretamente a eles. Entretanto, os fabricantes de dispositivos médicos não seriam capazes de atingir a conformidade com as normas, sem soluções de energia que tenham sido projetadas com aplicações médicas em mente.
Até recentemente, podia-se assumir que os dispositivos médicos seriam utilizados exclusivamente em instalações médicas dedicadas, como hospitais e clínicas. Tais instituições forneceram energia limpa dedicada para uso de seus dispositivos médicos mais sensíveis. Atualmente, os pacientes estão exigindo conveniência e as instalações médicas com recursos limitados significam que os dispositivos médicos estão sendo, cada vez mais, utilizados em casa. Aqui, questões como a compatibilidade eletromagnética (EMC) são de maior importância devido à prevalência de tecnologias como Bluetooth e Wi-Fi. Devido a isso, a última versão da norma (4ª edição) alterou os procedimentos de teste e os níveis de aceitação da EMC.
Outra introdução significativa foi a exigência de realizar uma avaliação de risco de acordo com a ISO 14971. O gerenciamento de risco é visto como um componente fundamental na demonstração da conformidade regulatória para os dispositivos médicos, assim a ISO 14971 define as melhores práticas para todas as fases do ciclo de vida de um dispositivo médico.
A Diretiva de Dispositivos Médicos aumenta ainda mais a carga de conformidade, exigindo que os fabricantes implementem um Sistema de Gerenciamento de Qualidade (QMS) que esteja em conformidade com a ISO 13485. A principal exigência é que uma organização (como um fabricante de fontes de alimentação) seja capaz de demonstrar sua capacidade de atender tanto os requisitos do cliente quanto os regulatórios de forma consistente.
Conversores CC/CC aprovados para uso médico, com classificação 2 x MOPP proporcionam flexibilidade
A abordagem típica para atingir a conformidade IEC 60601 é usar uma fonte de alimentação CA/CC que seja aprovada para uso médico. Entretanto, as aplicações com classificação BF também exigem que o instrumento AP atenda a classificação de 2 x MOPP. Muitas das fontes de alimentação CA/CC aprovadas para o mercado de medicina, atualmente, não têm uma classificação 2 x MOPP e não são apropriadas como uma solução de energia independente para aplicações onde a conformidade BF é necessária. Nesses casos, um conversor CC/CC com classificação 2 x MOPP e aprovado pela IEC 60601, suportará a conformidade BF para o AP. Outro exemplo comum são os aparelhos médicos que implementam uma capacidade de bateria reserva, devendo cumprir a classificação de 2 x MOPP durante uma falha de CA.
Os aparelhos médicos muitas vezes exigem várias tensões CC acionando o instrumento AP, que são diferentes da tensão CC do sistema principal fornecido. A fim de evitar o fornecimento de uma fonte de alimentação CA/CC personalizada, esta situação pode ser resolvida combinando conversores CC/CC com classificação 2 x MOPP e norma IEC 60601, junto com uma fonte de alimentação CA/CC com classificação ITE 60950, por exemplo. Outras vezes, a confiança da engenharia é simplesmente aumentada através da garantia de usar conversores CC/CC 2 x MOPP de grau médico para o instrumento AP, mesmo quando a fonte de alimentação CA/CC selecionada tem aprovação IEC 60601.
Os principais requisitos para 2 x MOPP (Figura 1) são 4000 VCA de isolação, 8 mm de distância do caminho de fuga e isolamento duplo. Os conversores CC/CC normalmente disponíveis (incluindo aqueles que possuem aprovação EN60950) oferecem entre 500 VCC a cerca de 1600 VCC de isolação e, portanto, não são adequados para aplicações médicas. Entretanto, estão disponíveis conversores CC/CC especiais que atenderão os requisitos da AP, quando usados em conjunto com tais fontes de alimentação padrões e prontas para uso.
Ao fornecer até 5000 VCA de isolação, isolamento duplo e 8 mm de distância do caminho de fuga através de seu transformador de isolação galvânica, um conversor CC/CC ainda pode proteger o paciente em caso de falha da fonte de alimentação CA/CC da rede, evitando assim o aparecimento de níveis de tensão de rede em qualquer ponto AP do paciente.
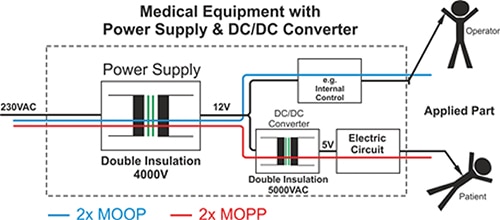
Figura 2: usando um conversor CC/CC para alcançar 2 x MOPP de proteção. (Fonte da imagem: TRACO Power)
Abordagem da TRACO para soluções de energia seguras para uso em medicina
No centro da abordagem da TRACO para fornecer soluções de energia de alto nível para a indústria médica está sua tecnologia de transformadores. Desenvolvido e aperfeiçoado durante um longo período, sua abordagem exclusiva garante a separação e a isolação necessárias, ao mesmo tempo em que consegue um acoplamento suficiente para permitir que o conversor CC/CC funcione de forma eficiente.
Uma baixa capacitância de acoplamento entre os enrolamentos primário e secundário do transformador é um aspecto importante da implementação da proteção. Valores tão baixos quanto 10-15 pF garantem que haja uma transferência insignificante de corrente através da barreira de isolação, fornecendo proteção ao paciente de acordo com os requisitos da IEC 60601.
A TRACO também implementa seu QMS de acordo com a ISO 13485, que abrange tanto o projeto quanto os processos de fabricação. Além disso, outras práticas além das exigências das normas garantem altos níveis de qualidade e segurança dentro de seus produtos.
Os componentes de grau industrial são selecionados e fornecidos para garantir a robustez do produto final. Como resultado, os dispositivos destinados ao uso em equipamentos de TI são impedidos pelas políticas internas da TRACO. A capacitação de mão-de-obra é garantida através da conformidade com a norma internacional IPC-A-610, onde a TRACO opera no nível 3, o nível mais alto de capacitação. Combinadas, estas medidas permitem à TRACO oferecer garantias de até 5 anos para alguns de seus produtos.
Como fabricante de soluções de energia em vez de dispositivos médicos, a TRACO não é obrigada a fornecer dados de avaliação de risco. Entretanto, o TRACO está em conformidade com a ISO 14971 e fornece arquivos de avaliação de risco cobrindo áreas cruciais, tais como ruptura de isolação, uso invertido de polaridade, efeitos de falha da ventoinha, inflamabilidade, choque mecânico, e muito mais para seus clientes. O fornecimento destes dados contribui, de forma significativa, para a avaliação de risco dos produtos médicos finais de seus clientes, poupando-lhes tempo e despesas durante o processo de projeto.
Uma oferta abrangente de produtos
A TRACO oferece soluções CA/CC e CC/CC para aplicações médicas, todas as quais atendem ao requisito de 2 x MOPP. Em conformidade com os requisitos EMC da IEC 60601-1 (4ª edição), elas são adequadas para todos os dispositivos médicos de peças aplicadas e conectadas a pacientes (em conformidade com a BF). Os produtos CA/CC variam de pequenos módulos de montagem em PCI de 5 W, uma gama de projetos de estrutura aberta de média potência e fontes de alimentação fechadas que oferecem níveis de potência de até 450 W.

Figura 3: a série TPP 40 da TRACO está disponível como estrutura aberta ou fechada. (Fonte da imagem: TRACO Power)
Todas as PSUs oferecem entrada de rede universal (85-264 VCA / 120-370 VCC) com correção do fator de potência ativa (PFC) acima de 100 W. A gama compreende saídas simples, duplas e triplas, cobrindo quase todos os requisitos de aplicação.
A linha de conversores CC/CC da TRACO compreende módulos de montagem em PCI com níveis de potência de 2 W a 30 W. Os dispositivos oferecem ambas as faixas de entrada 2:1 e 4:1 com entradas nominais disponíveis de 5 V, 12 V, 24 V e 48 V. As saídas simples e duplas são oferecidas a partir de 3,3 VCC a ±15 VCC.

Figura 4: a série THM de 15 watts é um conversor CC/CC de uso médico e montagem em PCI. (Fonte da imagem: TRACO Power)
Todos os conversores CC/CC da TRACO, com aprovação de uso médico, oferecem 5000 VCA rms de isolação entre entrada-saída que é dimensionado para uma tensão de trabalho de 250 VCA rms. Isto, junto com as correntes de fuga abaixo de 2 μA, as torna escolhas ideais para uso em conjunto com PSUs de CA/CC não aprovadas em aplicações médicas de segurança crítica.
Resumo
O mercado de serviços em saúde está crescendo e mudando rapidamente; e as normas aplicáveis, como a IEC 60601, estão em constante evolução para manter o ritmo. Os fabricantes de dispositivos médicos são os principais responsáveis por garantir a segurança dos pacientes e operadores de seus produtos. Entretanto, através de parcerias com fornecedores de energia elétrica experientes, os desafios e riscos podem ser reduzidos de forma significativa. Ao tirar proveito da equipe da TRACO, tais fabricantes obtêm acesso a produtos de alta qualidade, confiáveis e seguros, juntamente com um suporte abrangente e conhecedor no que diz respeito às normas médicas atuais.
Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.




